 Effets bénéfiques du peptide Chlorella-11 sur le blocage de l’activation des macrophages induite par le LPS et l’atténuation de l’inflammation induite par les blessures thermiques chez les rats.
Effets bénéfiques du peptide Chlorella-11 sur le blocage de l’activation des macrophages induite par le LPS et l’atténuation de l’inflammation induite par les blessures thermiques chez les rats.
On sait que lorsque l’on traite les bactéries à chlamydia, les bactéries relâchent des endotoxines LPS qui a un effet pire que la bactérie en elle même sur le court terme et provoque de l’inflammation souvent insupportable lors des traitement.
La Chlorella possède diverses activités biologiques remarquables. Un composant, le Val-Glu-Cys-Tyr-Gly-Pro-Asn-Arg-Pro-Gln-Phe (peptide Chlorella-11) s’est avéré capable de supprimer la production de NO induite par le LPS et l’inflammation.
Cherng JY1, Liu CC, Shen CR, Lin HH, Shih MF.
Informations sur l’auteur
Cependant, le mécanisme moléculaire derrière ces résultats et la cohérence entre les données in vitro et in vivo n’ont pas été étudiés. Les macrophages RAW 264.7 activés par les LPS ont été utilisés pour étudier les effets anti-inflammatoires moléculaires in vitro du peptide Chlorella-11.
Après activation, la production de NO et l’expression des protéines iNOS et NF-kappaB ainsi que de l’ARNm iNOS ont été mesurées en utilisant le dosage colorimétrique Griess, le transfert Western et la RT-PCR, respectivement. Les altérations des teneurs en PGE2 et en TNF-alpha ont également été contrôlées par ELISA. Pour des études in vivo, on a utilisé des rats Wistar à lésion thermique et des indications inflammatoires, par ex. la malondialdéhyde sérique (MDA), les niveaux de TNF-alpha et l’érythème cutané ont été évalués 48 h après la mise en place de la lésion. Les résultats in vitro ont montré que le peptide Chlorella-11 produisait une inhibition dépendante de la dose et du temps de la production de NO. L’inhibition efficace peut persister pendant au moins 6 heures après l’activation du LPS. Il a également été trouvé que l’expression de l’ARNm d’iNOS induite par le LPS, des protéines iNOS et NF-kappaB était diminuée par le traitement peptidique. Parallèlement, les niveaux de production de TNF-alpha et de PGE2 après l’activation du LPS ont également été inhibés. Ces résultats sont en accord avec les données in vivo selon lesquelles les taux sériques de MDA et de TNF alpha chez les animaux et l’érythème cutané chez les rats étaient considérablement réduits par rapport au groupe témoin (traité par solution saline). L’importance de cette étude met en lumière l’efficacité du peptide Chlorella-11 dans la prévention de la progression de l’inflammation in vitro et in vivo et son potentiel pour des applications cliniques.
Chlorella 11-peptide inhibe la production de molécules d’adhésion induites par les macrophages et réduit l’expression de l’endothéline-1 et la perméabilité endothéliale
Abstrait
Le processus inflammatoire dans les gros vaisseaux implique la régulation des molécules d’adhésion vasculaire telles que la sélectine des cellules endothéliales (E-sélectine), la molécule d’adhésion cellulaire intercellulaire-1 (ICAM-1) et la molécule d’adhésion cellulaire vasculaire-1 (VCAM-1). sont également connus comme les marqueurs de l’athérosclérose. Nous avons rapporté que le peptide 11 de Chlorella présentait des effets anti-inflammatoires efficaces. Ce peptide avec une séquence amino Val-Glu-Cys-Tyr-Gly-Pro-Asn-Arg-Pro-Gln-Phe a été davantage examiné pour son potentiel dans la prévention de l’athérosclérose dans cette étude. En particulier, les rôles du Chlorella 11-peptide dans l’abaissement de la production de molécules d’adhésion vasculaire, la protéine monocytaire chimioattractive (MCP-1) et l’expression de l’endothéline-1 (ET-1) des endothéliums (cellules SVEC4-10) ont été étudiés. La production de E-sélectine, ICAM-1, VCAM-1 et MCP-1 dans des cellules SVEC4-10 a été mesurée avec ELISA. L’expression de l’ARNm de ET-1 a été analysée par RT-PCR et gel d’agarose. Les résultats ont montré que Chlorella 11-peptide supprime de manière significative les niveaux de E-sélectine, ICAM, VCAM, MCP-1 ainsi que l’expression du gène ET-1. L’inhibition de la production de ICAM-1 et de VCAM-1 par le Chlorella 11-peptide a été inversée en présence d’inhibiteur de protéine kinase A (H89), ce qui suggère que la voie de l’AMPc était impliquée dans la cause inhibitrice du peptide. En outre, il a été montré que ce peptide réduit l’étendue de la perméabilité intercellulaire accrue induite par la combinaison de 50% de milieu de cellules RAW 264.7 activé par lipopolysaccharide (LPS) et 50% de milieu de culture cellulaire SEVC normal (appelé milieu conditionné à 50% de RAW). ). Ces données démontrent que Chlorella 11-peptide est une biomolécule prometteuse dans la prévention des maladies vasculaires inflammatoires chroniques.
1. Introduction
Les molécules d’adhésion circulantes (CAM) sont des protéines exprimées par l’endothélium vasculaire qui sont supposées jouer un rôle dans l’initiation du processus athérosclérotique. Il existe plusieurs familles de CAM, y compris les intégrines, les cadhérines, les sélectines et les membres de la superfamille des immunoglobulines [1]. Cependant, les molécules d’adhésion les plus importantes impliquées dans l’athérosclérose semblent être la molécule d’adhésion cellulaire intercellulaire-1 (ICAM-1), la sélectine des cellules endothéliales (E-sélectine) et la molécule d’adhésion des cellules vasculaires-1 (VCAM-1). Un taux élevé de ICAM-1 a montré une corrélation avec un risque accru d’événements cardiovasculaires [2]. Les niveaux d’E-sélectine sont en corrélation avec le risque de maladie cardiovasculaire (CVD) [3] et ont été utilisés avec succès pour prédire la sévérité de l’athérosclérose chez les patients [4]. VCAM-1 est un marqueur spécifique de l’athérosclérose avancée, car il est souvent exprimé dans les plaques d’athérosclérose [5]. Un niveau élevé de VCAM-1 est généralement associé à un risque accru d’événements coronariens chez les personnes atteintes de MCV existantes [2]. Des études indiquent également que la réduction du taux circulant de ces molécules d’adhésion pourrait réduire le risque de MCV [6]. La régulation positive des molécules d’adhésion sur les cellules endothéliales est importante après l’exposition de ces cellules à des molécules pro-inflammatoires telles que le facteur de nécrose tumorale (TNF) -α, l’interleukine (IL) -8 et la protéine chimioattractive monocytaire-1 (MCP-1). ) [7]. Initié par MCP-1, le recrutement et l’activation des monocytes / macrophages sont suivis et contribuent à l’initiation et la physiopathologie de la cardiopathie ischémique [8,9]. De plus, le MCP-1 serait impliqué dans le développement de l’athérosclérose [10], de la coronaropathie [11], du remodelage myocardique post-ischémique [12] et de l’insuffisance cardiaque [13]. La recherche sur la thérapie génique anti-MCP-1 a réussi à atténuer l’athérosclérose chez des souris déficientes en ApoE [14], ce qui suggère que la MCP-1 est une cible thérapeutique potentielle dans l’athérosclérose.
De plus, l’endothéline-1 (ET-1) sécrétée par les cellules endothéliales vasculaires agit comme un puissant vasoconstricteur endogène et joue un rôle important dans l’étiologie de la maladie vasculaire athéroscléreuse [15]. Lorsque les endothéliums sont sous inflammation, leur perméabilité intercellulaire accrue permettrait également l’absorption du cholestérol dans la paroi vasculaire [15]. Par conséquent, il a été démontré que la réduction de l’expression ET-1 élevée et de la perméabilité intercellulaire endothéliale restante à la normale constitue une approche efficace pour bloquer le développement de troubles circulatoires, y compris l’hypertension et l’athérosclérose [16].
Les algues vertes sont capables de prévenir l’hyperlipidémie induite par un régime riche en graisses [17] et l’athérosclérose chez les animaux de laboratoire [18]. De plus, Chlorella 11-peptide dérivé de l’algue verte démontre divers effets biologiques. Les composants du peptide 11 de Chlorella sont (Val-Glu-Cys-Tyr-Gly-Pro-Asn-Arg-Pro-Gln-Phe). Il a récemment été montré qu’il diminuait l’expression de l’oxyde nitrique synthase inductible (iNOS) et l’activité du facteur nucléaire-kappa-B (NF-κB) et possédait des propriétés antioxydantes [19,20]. Puisque l’athérosclérose est connue pour être associée à un cholestérol élevé et à une inflammation chronique [21], l’examen des relations entre les molécules d’adhésion, MCP-1, ET-1, l’intégrité de la membrane endothéliale avec Chlorella 11-peptide aiderait à explorer leur potentiel thérapeutique. athérosclérose. Dans cette étude, le surnageant de culture RAW264.7 stimulée par LPS a été ajouté aux cellules endothéliales (SVEC4-10) pour la stimulation de ces cellules. En effet, l’activation des macrophages produit des cytokines pro-inflammatoires nécessaires au développement de l’athérosclérose [22]. Après les stimuli de SVEC4-10, les réponses des endothéliums avec et sans Chlorella 11-peptide ont ensuite été évaluées.
2. Résultats et discussion
2.1. Effets Inhibiteurs Du Chlorella 11-Peptide Sur La Production De MCP-1 Induite Par Le LPS Dans Les Macrophages RAW264.7
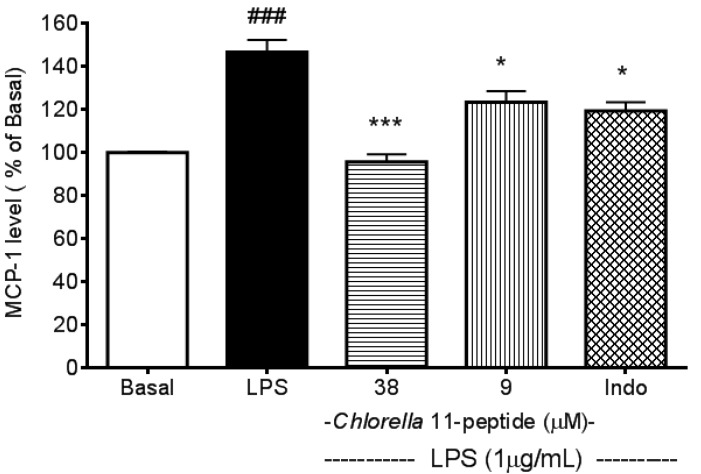
La différence de production de MCP-1 entre les groupes traités par LPS et les groupes de base a atteint un maximum à 12 h après la stimulation par le LPS [23].
Par conséquent, ce point de temps a été choisi pour une étude plus approfondie (p <0,005, figure 1). La production de MCP-1 induite par le LPS était significativement inhibée (p <0,005 et p <0,05) par le Chlorella 11-peptide (38 μM et 9 μM, respectivement). L’indométhacine, un anti-inflammatoire non stéroïdien, a également montré une inhibition de la production de MCP-1 induite par le LPS. L’effet inhibiteur de l’indométhacine (0,25 mM) sur la production de MCP-1 s’est avéré similaire à celui de Chlorella 11-peptide dans une faible dose (9 μM) mais moins puissant que dans une forte dose (38 μM) de Chlorella 11 -peptide.
Des études ont montré que le LPS induit la production de cytokines pro-inflammatoires (TNF-α, IL-1, IL-6) qui contribuent à l’inflammation vasculaire et à l’athérosclérose [19] et l’apparition de l’athérosclérose par adhérence des monocytes aux cellules endothéliales activées [21]. Dans la présente étude, nous avons constaté que LPS induit significativement la production de MCP-1 dans les macrophages à 12 h (Figure 1). Par conséquent, le surnageant de cellules de macrophages stimulées par LPS cultivées à 12 h a été appliqué pour induire des molécules d’adhésion dans les cellules endothéliales SVEC4-10 et ces molécules induites par rapport au peptide 11 de Chlorella peuvent ensuite être évaluées.
2.2. Effets Inhibiteurs De Chlorella 11-Peptide Sur E-sélectine, ICAM-1 Et VCAM-1 Production Induite Par 50% RAW-Conditionné Moyen
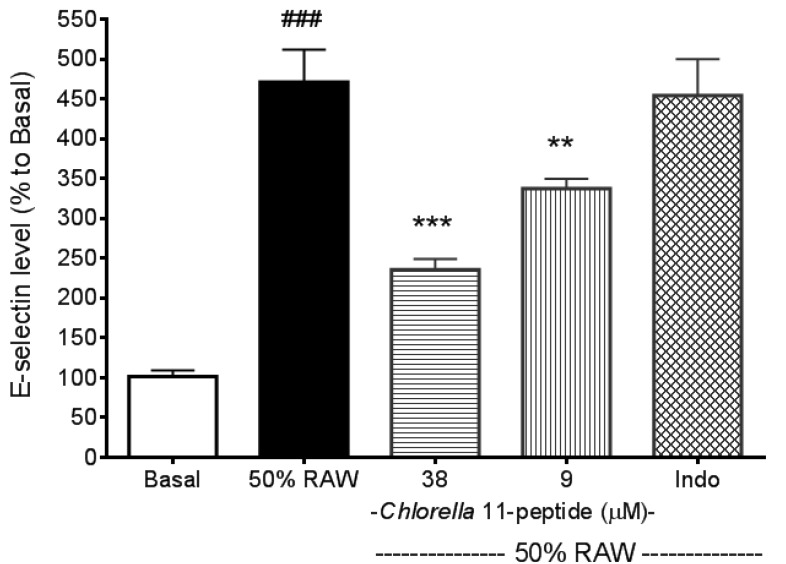
La MCP-1 recombinée et d’autres cytokines pro-inflammatoires (TNF-α et IL-6 recombinés), comme mentionné dans l’introduction du manuscrit, sont capables d’induire des molécules d’adhésion. Ces preuves ont toutes été bien démontrées par le travail des autres et ont été testées dans nos expériences préliminaires (données non montrées). De plus, dans nos expériences, nous avons également trouvé que le milieu RAW traité au Chlorella 11-peptide n’était pas capable d’induire la production de molécules d’adhésion comme témoin (données non montrées). La production d’E-sélectine dans les cellules endothéliales SVEC4-10 a été significativement induite par un milieu conditionné RAW à 50% (p <0,005, Figure 2). Les concentrations élevées (38 μM) et faibles (9 μM) de Chlorella 11-peptide ont été capables de diminuer significativement la production d’E-sélectine (p <0,005 et p <0,01, respectivement). Cependant, l’indométhacine n’a pas affecté la production de E-sélectine induite par 50% de milieu conditionné RAW. Il y avait environ une augmentation de 5 fois dans la production de ICAM-1 lorsque les cellules endothéliales SVEC4-10 ont été stimulées avec 50% de milieu conditionné RAW (figure 3). La production accrue d’ICAM-1 était significativement inhibée par le Chlorella 11-peptide et l’indométhacine (p <0,005, Figure 3). VCAM-1 production a également été induite avec 50% de milieu conditionné RAW (figure 4). Notamment, ni la faible concentration de 11-peptide de Chlorella ni l’indométhacine ne présentaient d’inhibition sur l’induction de VCAM-1. Cependant, la forte concentration de Chlorella 11-peptide a significativement supprimé la production de VCAM-1 (p <0,005).
Normalement, l’E-sélectine exprimée par les cellules endothéliales est faible, mais les cytokines, les espèces réactives de l’oxygène et l’endotoxine bactérienne peuvent provoquer son expression [24]. ICAM-1 est exprimée constitutivement sur les cellules endothéliales dans la plupart des lits vasculaires régionaux, et son expression peut être significativement augmentée avec des cytokines ou des endotoxines bactériennes. En comparaison avec ICAM-1, VCAM-1 médie principalement l’adhésion des lymphocytes et des monocytes lors de la stimulation [25]. Amberger et al. ont rapporté une faible expression du gène VCAM-1 des cellules endothéliales de la veine ombilicale humaine après stimulation par le TNF-α [26]. Il est important de noter que toutes ces molécules d’adhésion élevées en relation positive avec l’athérosclérose ont été substantiellement réduites par la présence du peptide 11 de Chlorella (38 uM). L’indométhacine est un puissant agent anti-inflammatoire. Cependant, ses effets inhibiteurs sur les molécules d’adhérence induites par les cytokines pro-inflammatoires (par exemple E-sélectine, VCAM-1) n’étaient pas aussi efficaces que ceux illustrés à la Figure 2 et Figure 4. De plus, comparé à l’indométhacine (Figure 4) peut efficacement soulager à la fois la production de ICAM-1 et VCAM-1 qui sont responsables de la transmigration des leucocytes (ICAM-1) et la transduction du signal leucocyte-endothélium (VCAM-1) [27,28].
L’AMP cyclique est un régulateur omniprésent des réactions inflammatoires et immunitaires. La médiation de la communication croisée de cellules par l’intermédiaire de molécules d’adhésion (par exemple, ICAM-1, E-sélectine, VCAM-1) a été rapportée comme étant dépendante de l’AMPc intracellulaire [29, 30, 31]. Dans cette étude, nous avons utilisé un inhibiteur de la protéine kinase A, H89 [26], pour étudier si les effets inhibiteurs de Chlorella 11-peptide sur la production de ICAM-1 et VCAM-1 ont été médiés via la voie de l’AMPc. Nous avons montré que l’addition de H89 peut compromettre les effets inhibiteurs de Chlorella 11-pepetide sur la production de ICAM-1 et VCAM-1 induite (Figure 3 and Figure 4). Cela indique que la voie de l’AMPc était probablement impliquée dans les actions inhibitrices du peptide. La réaction de H89 à l’indométhacine sur la production de VCAM-1 induite n’a pas été observée (figure 4). L’explication possible est que l’indométhacine nécessite une concentration beaucoup plus élevée (supérieure à 20 mM) pour inhiber l’activité de la protéine kinase AMPc dépendante [32], ce qui est beaucoup plus élevé que la concentration (0,25 mM) utilisée dans cette étude.
2.3. Effets Inhibiteurs De Chlorella 11-Peptide Sur L’expression Génique De L’endothéline-1
L’addition de 50% de milieu conditionné par RAW a fortement induit l’expression de l’ARNm de l’endothéline-1 (ET-1) dans les cellules endothéliales SVEC4-10 (p <0,005, figure 5). Cette induction de l’expression du gène ET-1 peut être significativement inhibée par la forte dose de Chlorella 11-peptide (p <0,005) et d’indométhacine (p <0,01).
L’expression de l’ARNm de l’ET-1 était élevée dans l’artère avec une lésion athéroscléreuse [16]. L’antagonisme des récepteurs ET-1 a permis de réduire la formation de lésions athéroscléreuses [33]. Ainsi, le blocage de l’ET-1 a été considéré comme une stratégie de prévention de l’athérosclérose [15]. Dans cette étude, les données ont montré que Chlorella 11-peptide est capable de supprimer de manière significative l’expression de l’ARNm ET-1 et détient un grand potentiel dans les utilisations anti-athérosclérose.
2.4. Effets Inhibiteurs De Chlorella 11-Peptide Sur La Perméabilité Intercellulaire De L’endothélium
Après des stimuli de 50% de milieu conditionné RAW, la perméabilité intercellulaire endothéliale SVEC4-10 a montré une forte augmentation (p <0,005, figure 6). Les doses élevées et faibles de Chlorella 11-peptide ont inhibé l’augmentation de la perméabilité intercellulaire (p <0,005). De plus, cette inhibition de la perméabilité intercellulaire n’a pas été observée dans le groupe traité par l’indométhacine.
La perméabilité endothéliale est contrôlée en partie par l’ouverture et la fermeture dynamiques des jonctions cellule-cellules endothéliales qui se rapportent aux interactions entre les cellules endothéliales et la matrice extracellulaire [34,35]. L’augmentation de la perméabilité endothéliale aux lipoprotéines ou aux cellules immunitaires est considérée comme une étape initiatrice de la pathogenèse de l’athérosclérose, et l’accumulation de débris dans l’intima conduirait à des plaques athérosclérotiques [21]. Par conséquent, le maintien de la perméabilité endothéliale non affectée par les cellules pro-inflammatoires aiderait à diminuer la formation de plaque [36]. Notre test de perméabilité a montré que Chlorella 11-peptide possède une puissante capacité à inhiber la perméabilité intercellulaire accrue de l’endothélium SVEC4-10 induite par 50% de milieu conditionné RAW (Figure 6), ce qui indique l’efficacité du peptide dans la prévention du développement de l’athérosclérose .
Aller à:
3. Section expérimentale
3.1. Matériaux
Le milieu aigle modifié de Dulbecco (DMEM), le pyruvate de sodium et l’acide aminé non essentiel ont été achetés chez Gibco BRL (Taipei, Taiwan). L’indométhacine (I17378), la papaïne, la pepsine, le réactif de Bradford (B6919) et H89 ont été achetés auprès de Sigma (Taipei, Taiwan). Le flavourzyme de type A et l’alcalase ont été achetés auprès de Novo Nordisk (Taipei, Taiwan). Un système de miniprep à ARN total (Viogene BioTek Corporation, Taipei, Taiwan) et Access RT-PCR (Promega, Madison, WI, USA) ont été utilisés pour la RT-PCR. Les kits d’analyse ELISA MCP-1, VCAM, ICAM et E-selectine étaient des produits de systèmes de R & D (Taipei, Taiwan). Tous les produits chimiques ont été dissous dans de l’eau déminéralisée stérilisée à l’exception de l’indométhacine dans de l’éthanol aqueux à 95% et de la pepsine dans du HCl 10 mM froid (4 mg ml « 1).
3.2. Chlorella-11 Préparation du peptide
Le peptide Chlorella-11 de Chlorella pyrenoidosa a été préparé à partir de déchets de protéines algales essentiellement comme décrit précédemment [19,20]. Les déchets de protéines algales ont été obtenus à partir du matériau insoluble après extraction à l’eau chaude de Chlorella pyrenoidosa. Ensuite, les déchets de protéines algales (10%, p / v) ont été digérés avec des protéases commerciales (pepsine, flavourzyme, alcalase et papaïne) à la concentration de 0,2% (p / v) pendant 15 h au pH et à la température indiqués pour chaque réaction enzymatique, en utilisant les conditions de réaction fournies par le fabricant. A la fin de la réaction, la digestion a été chauffée dans un bain d’eau bouillante pendant 10 minutes afin d’inactiver l’enzyme. Le matériau non soluble résultant a ensuite été séché par pulvérisation et a été extrait avec du methanol (1:10 p / v) pendant trois fois. Après avoir été concentrée, la fraction extraite au MeOH a été ensuite extraite à nouveau avec de l’eau distillée avant la lyophilisation.
L’isolement et la purification du Chlorella 11-peptide étaient tels que décrits précédemment avec modification [19,20]. Brièvement, du sulfate d’ammonium a été ajouté pour précipiter les protéines et les protéines précipitées ont été éliminées par centrifugation (10 000 x g, 30 min) et dissoutes dans un petit volume d’eau distillée. La solution a été fractionnée en utilisant une colonne HR de Sephacryl S-100 (φ 2,6 x 70 cm) pour détecter les peptides à 210 nm. La fraction a été recueillie et ensuite chargée sur une colonne Q-Sepharose Fast Flow (φ 2,6 x 40 cm), qui a été pré-équilibrée avec une solution tampon Tris-HCl 20 mM (pH 7,8). La séparation a été effectuée avec du NaCl 1,0 M dans la même solution tampon et les fractions ont été recueillies, dialysées dans de l’eau désionisée et lyophilisées. La concentration en peptide a été déterminée avec un dosage de protéines Pierce micro BCA (Thermo Fisher Scientific Inc., Waltham, MA, USA). Le poids moléculaire des peptides a été déterminé en utilisant une colonne Superdex peptide HR 10/30 à un débit de 0,5 ml / min. La courbe standard a été établie avec le cytochrome c (MW 12327 Da), l’approtonine (MW 6500 Da), la gastrine (MW 2098 Da) et Leu-Gly (MW 188 Da).
La fraction peptidique a été en outre séparée successivement par une colonne HPLC en phase inverse, et un peptide purifié a été atteint. La pureté et l’identité de la préparation finale ont été confirmées par analyse spectrométrique de masse sur spectromètre de masse Q-TOF Agilent 6510 (> 95%) et dégradation d’Edman (voir Informations supplémentaires). La séquence de 11-peptide de Chlorella a été déterminée comme Val-Glu-Cys-Tyr-Gly-Pro-Asn-Arg-Pro-Gln-Phe, avec une masse moléculaire de 1309 Da. Dans les dernières parties de notre travail, nous avons utilisé le peptide synthétique fourni par Kelowna International Scientific Inc. (Taiwan).
3.3. RAW264.7 Culture de macrophages
Les macrophages RAW264.7 (numéro ATCC: TIB-71) ont été obtenus auprès de Bioresource Collection & Research Centre (Taiwan) et cultivés dans du DMEM additionné de 10% de sérum fœtal bovin (Hyclone), 2 mM de glutamine, 1% d’acide aminé non essentiel. , 25 mM d’HEPES, 1 mM de pyruvate de sodium, 100 U / ml de pénicilline et 100 ug / ml de streptomycine. Les cellules ont été cultivées et maintenues dans des flacons de 75 T (1 x 107 cellules / boîte) à 37 ° C dans une atmosphère humidifiée contenant 5% de C02.
3.4. MCP-1 Assay
Les cellules RAW264.7 ont été ensemencées à une densité de 2 x 104 cellules / puits dans des plaques à 96 puits. Ensuite, les cellules ont été incubées en présence de LPS (1 ug / ml) avec / sans peptide 11 de Chlorella (9 uM et 38 uM) pendant 12 heures avant de recueillir le milieu de culture pour la mesure de MCP-1. Ce surnageant de culture (sans traitement peptidique) a également été prélevé pour préparer un « milieu RAW-conditionné à 50% » (voir la section suivante). La gamme de concentration de Chlorella 11-peptide a été choisie sur la base de notre découverte précédente [19]. L’indométhacine (0,25 mM) a été utilisée comme témoin positif. Les niveaux de MCP-1 dans les milieux de culture ont été déterminés avec des kits de dosage ELISA commerciaux.
3.5. Molécules d’adhésion – E-sélectine, mesures de niveau ICAM-1 et VCAM-1 dans les cellules endothéliales SVEC4-10
Les cellules SVEC4-10 (numéro ATCC: CRL-2181), qui sont bien différenciées, réagissent comme les cellules endothéliales normales à certaines interleukines et aux signaux de la matrice extracellulaire pour la différenciation en tube. Il a été démontré que la SVEC4-10 conservait les caractéristiques morphologiques et fonctionnelles de la CE normale [37]. Les cellules endothéliales SVEC4-10 ont été obtenues auprès de Bioresource Collection & Research Center (Taiwan) et cultivées dans du milieu Eagle modifié par Dulbecco (DMEM) additionné de 10% de sérum fœtal bovin, 1 mM de pyruvate de sodium, 100 U / ml de pénicilline et 100 μg / mL de streptomycine. . Les cellules ont été maintenues dans des boîtes de Pétri de 100 mm à 37 ° C dans une atmosphère humidifiée contenant 5% de C02. Les cellules SVEC4-10 ont été ensemencées à une densité de 2 x 104 cellules / puits dans des plaques à 96 puits pendant une nuit avant les traitements. Pour les stimuli, le milieu de culture des cellules SVEC4-10 a été changé en « milieu RAW-conditionné à 50% » (à volume égal de milieu SVEC4-10 et surnageant de milieu de culture RAW264.7 stimulé par LPS) avec et sans Chlorella. -peptide. L’indométhacine a été dissoute dans de l’éthanol à 95% et appliquée en tant que contrôle positif et les cellules ont été incubées pendant 24 h supplémentaires avant les dosages E-sélectine et ICAM-1 et 6 heures avant le dosage VCAM-1. La concentration de ces molécules d’adhésion a été mesurée avec des kits de dosage ELISA du commerce.
3.6. Analyse de l’ARNm de l’endothéline-1 par transcription inverse – réaction en chaîne de la polymérase (RT-PCR)
Les cellules endothéliales SVEC4-10 (2 x 105 cellules / ml) dans une boîte de 100 mm ont été stimulées avec un milieu conditionné à 50% de RAW en présence de Chlorella 11-peptide et incubées pendant 24 h. L’ARN total a été extrait en utilisant un kit d’isolement d’ARN GENTRA (R-5000A, Minneapolis, MN, USA). L’ARN a été soumis à une transcription inverse en utilisant un kit de synthèse d’ADNc de premier brin pour la RT-PCR (système Access RT-PCR, Promega, Madison, WI, USA). Une PCR semi-quantitative a été réalisée en utilisant des amorces pour l’ET-1 de souris (forward, 5′-AAGCGCTGTTCCTGTTCTTCA-3 ‘, reverse, 5′-CTTGATGCTATTGCTGATGG-3′) et le gène d’entretien β-actine (forward, 5’-GTGGGCCGCTCAGGCCA-3 ‘ ; inverse, 5’-CTCAGCTGTGGTGGTGAAGC-3 ‘). Les produits de réaction ont été examinés par électrophorèse dans un gel d’agarose à 1% et visualisés avec du bromure d’éthidium. L’analyse densitométrique a été réalisée en utilisant le système de documentation et d’analyse Alpha Imager 2000 (Alpha Innotech Corporation, San Leandro, CA, USA).
3.7. BSA Transwell Permeability Assay
Les cellules SVEC4-10 ont été ensemencées (1 x 105 cellules / insert) sur des filtres en polystyrène enrobés de gélatine (1%) (Costar Transwell, taille des pores = 0,4 mm, Corning Inc., Taiwan), laissés à confluence sur des inserts Transwell et puis remplacé par du milieu sans FBS pendant 3 h supplémentaires [38]. Un milieu exempt de FBS contenant 10 mg / ml de BSA a été placé dans le compartiment supérieur et un milieu exempt de FBS sans BSA a été placé dans le compartiment inférieur du Transwell. La vitesse de transfert à travers la monocouche cellulaire a été évaluée en mesurant la quantité accrue de BSA dans le compartiment inférieur après 30 min. La BSA a été quantifiée en utilisant le réactif de Bradford.
3.8. Analyses statistiques
Les données des résultats (n ≥ 8) de différents jours expérimentaux ont été analysées statistiquement pour MCP-1, E-sélectine, ICAM-1, VCAM-1 et les tests de perméabilité intercellulaire en utilisant le logiciel Prism (GraphPAD Inc., La Jolla, CA, USA). ). Un test non apparié de Student à deux queues a été appliqué pour comparer les valeurs moyennes de deux populations de données continues. La distribution normale et la variance de chaque groupe étaient les mêmes. Des données de gel d’électrophorèse ont été réalisées (n ≥ 3) et un exemple représentatif est montré dans les résultats.
Aller à:
4. Conclusions
L’expression de diverses CAMs par des cellules endothéliales activées est une étape déterminante de la vitesse dans le recrutement des cellules inflammatoires et joue un rôle central dans la progression de CVD [6, 24]. Notre étude précédente a clairement montré que les peptides de Chlorella sont un inhibiteur très efficace de la production de TNF-α et d’IL-6 dans les macrophages [19]. Dans cette étude, nous démontrons en outre que Chlorella 11-peptide pourrait non seulement empêcher la production de MCP-1 induite par le LPS dans les macrophages RAW264.7, mais aussi inhiber efficacement la production de molécules d’adhésion dans les cellules endothéliales. De plus, ce peptide s’est montré capable de soulager l’expression de l’ARNm de l’ET-1 et de maintenir la perméabilité endothéliale non affectée sous l’influence des cytokines pro-inflammatoires. En combinant ces résultats, Chlorella 11-peptide peut devenir une biomolécule potentielle dans l’amélioration du développement de l’athérosclérose.
Aller à:
Remerciements
Nous sommes très reconnaissants au Conseil national des sciences de Taïwan (NSC 101-2113-M-194-002) et à l’hôpital de la ville de Taipei de Taiwan pour le financement de la recherche.
Les auteurs ne déclarent aucun conflit d’intérêt.
- Review The role of adherens junctions and VE-cadherin in the control of vascular permeability.[J Cell Sci. 2008]
- Review Signaling mechanisms regulating endothelial permeability.[Physiol Rev. 2006]
- Review Atherosclerosis is an inflammatory disease.[Am Heart J. 1999]
- Nonmuscle myosin light-chain kinase deficiency attenuates atherosclerosis in apolipoprotein E-deficient mice via reduced endothelial barrier dysfunction and monocyte migration.[Circulation. 2011]
- Beneficial effects of Chlorella-11 peptide on blocking LPS-induced macrophage activation and alleviating thermal injury-induced inflammation in rats.[Int J Immunopathol Pharmacol. 2010]
- Anticancer and antioxidant activities of the peptide fraction from algae protein waste.[J Agric Food Chem. 2010]
- Beneficial effects of Chlorella-11 peptide on blocking LPS-induced macrophage activation and alleviating thermal injury-induced inflammation in rats.[Int J Immunopathol Pharmacol. 2010]
- Anticancer and antioxidant activities of the peptide fraction from algae protein waste.[J Agric Food Chem. 2010]
- Telmisartan increases the permeability of endothelial cells through zonula occludens-1.[Biol Pharm Bull. 2009]
- Review Vascular protectants for the treatment of atherosclerosis.[Expert Rev Cardiovasc Ther. 2003]
- Review Adhesion molecules and their role in vascular disease.[Am J Hypertens. 2001]
- Beneficial effects of Chlorella-11 peptide on blocking LPS-induced macrophage activation and alleviating thermal injury-induced inflammation in rats.[Int J Immunopathol Pharmacol. 2010]

Commentaires récents